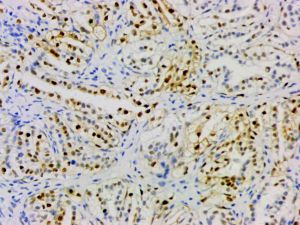
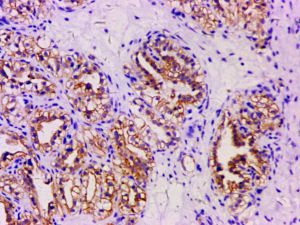
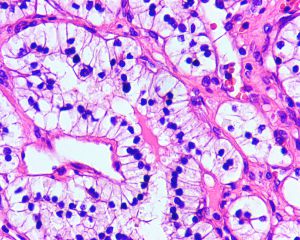
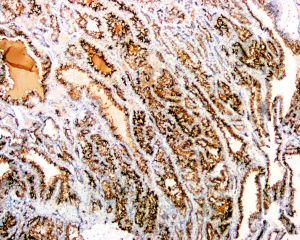
几乎全部阳性(≥95%的病例阳性):
CA9、CAIX、PAX8通常阳性(<95%,≥75%的病例阳性):
34bE12、GLUT1、CK7、SMA有时阳性(<55%,≥35%的病例阳性):
CD10少数阳性(<35%,≥15%的病例阳性):
P21、RCC偶尔阳性(<15%,≥5%的病例阳性):
Desmin几乎全部阴性(<5%的病例阳性):
PRP、P504s、TFE32. 肿瘤常位于肾皮质,一般较小,界清,有包膜,常伴囊性变,偶尔呈多灶性或双侧发生;
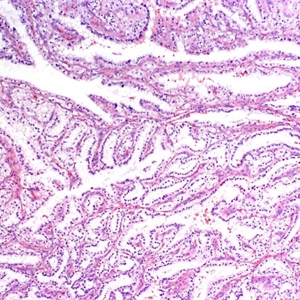
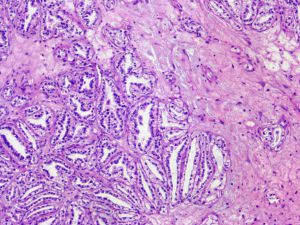
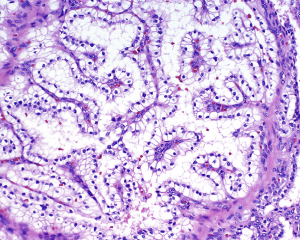
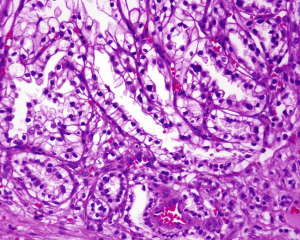
3. 镜下瘤细胞呈乳头状、管状、腺泡状、囊性以及实性等多种结构不同比例混合;常见分支小管以及起源于囊肿的分支乳头结构;
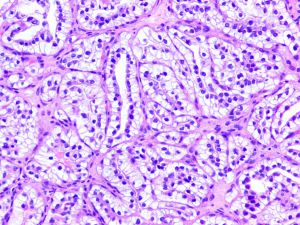
4. 肿瘤细胞立方-低柱状,细胞核呈一致的圆形,远离基底膜呈线性排列(类似于“鲨鱼的牙齿”),核仁通常不明显(ISUP分级1-2级核);胞浆透亮;偶尔可见大细胞成分或IUSP核分级3级的核;
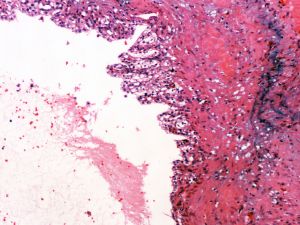
5. 腺腔内常见嗜酸性分泌物;
6. 可见多少不等的纤维性或平滑肌性间质,部分病例以平滑肌成分为主(以前称为血管平滑肌腺瘤样肿瘤);
7. 无坏死,罕见肾周脂肪浸润,无血管侵犯。
8.偶尔可发生高级别转化或去分化
9.基于透明细胞乳头状肾细胞癌具有明显较好的预后,特别是好于透明细胞肾细胞癌和乳头状肾细胞癌,因此诊断标准应该严格(要求形态学和免疫表型特点均符合方可诊断)
透明细胞肾细胞癌:瘤细胞胞浆更丰富,无分支乳头状排列,偶尔可见瘤细胞核远离基底部的线性排列,免疫组化染色弥漫膜表达CAIX和CD10,通常不表达或仅仅偶尔表达CK7,遗传学可见3p缺失;
乳头状肾细胞癌:以乳头状和管状结构为主,胞浆常常嗜酸性为主,乳头轴心可见泡沫样组织细胞聚集以及砂粒体钙化,常见坏死。免疫组化染色弥漫表达AMACR/p504s和CD10,一般不表达CAIX;
TFE3易位性肾细胞癌:透明细胞和乳头状排列,瘤细胞核仁明显,核级别高,常见砂粒体钙化或色素沉积,免疫组化染色核特征性表达TFE3,弥漫表达CD10;
低度恶性潜能多房囊性肾肿瘤:可与广泛囊性变的透明细胞乳头状肾细胞癌混淆,两者均可弥漫表达CK7,但与透明细胞乳头状肾细胞癌表达ck34be12不同,低度恶性潜能多房囊性肾肿瘤弥漫表达CD10和CAIX;
混合性上皮间质肿瘤:可与伴有明显平滑肌间质的透明细胞乳头状肾细胞癌混淆,前者可见卵巢样间质,除了表达平滑肌标志之外,常弥漫表达ER和PR。
结节性硬化在相关的乳头状肾细胞癌:可见透明细胞和乳头状排列,免疫组化染色弥漫表达CK7和CD10以及CAIX,胞浆内可见致密而圆形的嗜酸性小球,与结节性硬化症相关可资鉴别。
1.Zhou H, Zheng S, Truong L D, et al. Clear cell papillary renal cell carcinoma is the fourth most common histologic type of renal cell carcinoma in 290 consecutive nephrectomies for renal cell carcinoma [J]. Hum Pathol, 2014, 45(1): 59-64.
2.Williamson S R, Eble J N, Cheng L, et al. Clear cell papillary renal cell carcinoma: differential diagnosis and extended immunohistochemical profile [J]. Mod Pathol, 2013, 26(5): 697-708.
3.Deml K F, Schildhaus H U, Comperat E, et al. Clear Cell Papillary Renal Cell Carcinoma and Renal Angiomyoadenomatous Tumor: Two Variants of a Morphologic, Immunohistochemical, and Genetic Distinct Entity of Renal Cell Carcinoma [J]. Am J Surg Pathol, 2015, 39(7): 889-901.
4.Aron M, Chang E, Herrera L, et al. Clear Cell-Papillary Renal Cell Carcinoma of the Kidney Not Associated With End-stage Renal Disease: Clinicopathologic Correlation With Expanded Immunophenotypic and Molecular Characterization of a Large Cohort With Emphasis on Relationship With Renal Angiomyoadenomatous Tumor [J]. Am J Surg Pathol, 2015, 39(7): 873-88.
5. Fadi Brimo, Chantal Atallah, Gangyong Li & John R Srigley. Cystic clear cell papillary renal cell carcinoma: is it related
to multilocular clear cell cystic neoplasm of low malignant potential?Histopathology. 2016 Apr;68(5):666-72.
6. Do Clear Cell Papillary Renal Cell Carcinomas Have Malignant Potential? Diolombi ML et al. Am J Surg Pathol. (2015)
7. Dhakal HP, McKenney JK, Khor LY, Reynolds JP, Magi-Galluzzi C, Przybycin CG.Renal Neoplasms With Overlapping Features of Clear Cell Renal Cell Carcinoma and Clear Cell Papillary Renal Cell Carcinoma: A Clinicopathologic Study of 37 Cases From a Single Institution.Am J Surg Pathol. 2016 Feb;40(2):141-54.